On constate un aspect infiltré de la face antérieure de l’avant-bras gauche, une peau cartonnée avec un aspect dit en « peau d’orange ». La pression de l’avant-bras gauche est douloureuse. Les articulations ne sont ni douloureuses ni gonflées.
[[asset:image:7339 {"mode":"full","align":"","field_asset_image_copyright":["DR"],"field_asset_image_description":[]}]]Devant l’hypothèse initiale d’un érésipèle de l’avant-bras gauche et afin d’éliminer une collection sous cutanée, une échographie est réalisée : elle rapporte un aspect de fasciite de la loge antérieure des muscles de l’avant-bras gauche prédominant sur le bord radial (figure 1a).
[[asset:image:7340 {"mode":"full","align":"","field_asset_image_copyright":["DR"],"field_asset_image_description":["Figure 1a"]}]]Une IRM de l’avant-bras gauche confirme l’épaississement des fascias prédominant sur la loge antérieure de l’avant-bras, plus marqué autour des tendons extenseurs radiaux du carpe, du long palmaire et des fléchisseurs profonds. Il n’y a pas de myosite (figures 1b).
[[asset:image:7341 {"mode":"small","align":"","field_asset_image_copyright":["DR"],"field_asset_image_description":["Figure 1b"]}]][[asset:image:7342 {"mode":"small","align":"","field_asset_image_copyright":["DR"],"field_asset_image_description":["Figure 1b"]}]]Un syndrome confirmé par une éosinophilie marquée
Le diagnostic de syndrome de Shulman ou fasciite avec éosinophilie est évoqué, le patient est hospitalisé. La NFS réalisée à l’admission confirme la présence d’une éosinophilie marquée (3,44 g/l), sans autre anomalie. La CRP est élevée (42 mg/l) et il existe une hypergammaglobulinémie polyclonale. La fonction rénale est normale ainsi que le bilan hépatique. La recherche d’anticorps est négative : AAN, ADN natifs, FR, ACPA, ANCA.
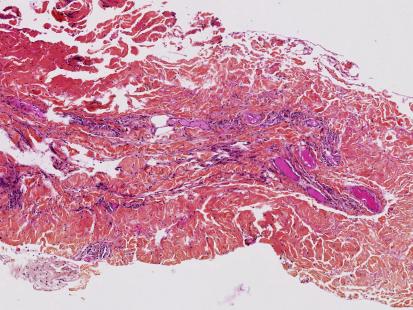
Une biopsie chirurgicale du fascia est réalisée. L’examen anatomopathologique de la pièce montre un discret infiltrat inflammatoire périvasculaire comportant quelques éosinophiles (figures 2).
[[asset:image:7343 {"mode":"full","align":"","field_asset_image_copyright":["DR"],"field_asset_image_description":["Figure 2 : Infiltrat inflammatoire tr\u00e8s mod\u00e9r\u00e9, principalement p\u00e9ri-vasculaire et discr\u00e8tement interstitiel"]}]][[asset:image:7344 {"mode":"full","align":"","field_asset_image_copyright":["DR"],"field_asset_image_description":["Figure 2 : Infiltrat fait de petits lymphocytes sans atypie et de quelques polynucl\u00e9aires \u00e9osinophiles. \r\nAbsence de granulome et de prolif\u00e9ration tumorale.\r\n"]}]]Le diagnostic de fasciite avec éosinophilie est confirmé. Le patient n’a aucune complication de l’éosinophilie chronique.
Un traitement par ivermectine, prednisone puis méthotrexate
Après un traitement par ivermectine, un traitement par prednisone 0,7 mg/kg/jour (soit 80 mg) a été introduit. La décroissance a été entreprise à 15 jours. Lors de la première réévaluation à 3 semaines, il persistait cependant des douleurs apparues à l'initiation de la décroissance de la corticothérapie, malgré une amélioration de l’aspect cutané. À visée d'épargne cortisonique, un traitement par méthotrexate 15 mg/semaine per os a alors été introduit permettant une mise en rémission complète du patient.
Discussion : un syndrome rare à signes cutanés évocateurs, traité par corticothérapie
Shulman a décrit en 1974 les deux premiers cas associant une induration des tissus sous-cutanés avec limitation des amplitudes articulaires, une éosinophilie et une hypergammaglobulinémie. Ce syndrome rare est parfois déclenché à la suite d’un effort inhabituel, d’un traumatisme ou après certains médicaments (statines, fosinopril, héparine).
Les signes cutanés sont évocateurs, surtout s’ils sont bilatéraux et siègent aux avant-bras : œdème induré, douloureux (prenant ou non le godet) remplacé progressivement par une induration sclérodermiforme, donnant un aspect en « peau d’orange ». Dans les formes plus évoluées, l’examen cutané peut mettre en évidence un aspect dit en « veines en creux » reflétant une fibrose profonde. Les myalgies sont fréquentes, parfois associées à des polyarthralgies inflammatoires des synovites distales. Si le syndrome de Shulman ne s’accompagne habituellement pas de manifestation viscérale, ni d’éosinophilie chronique, il est possible d’observer un syndrome du canal carpien.
L’éosinophilie sanguine est l’anomalie biologique la plus fréquente, rencontrée chez plus de 60 % des patients, et associée à une hypergammaglobulinémie polyclonale. Il est aussi possible d’observer une élévation de la VS, de la CRP ou des CPK devant faire rechercher une atteinte musculaire. La recherche d’anticorps anticytoplasme des polynucléaires neutrophiles (ANCA), ou de facteur rhumatoïde (FR) est habituellement négative. Les anticorps antinucléaires sont positifs chez 15 à 20 % des patients, sans anticorps anti-ADN natifs ou anticorps anti-antigènes solubles. Leur présence doit faire rechercher un diagnostic différentiel (sclérodermie systémique, syndrome d’éosinophilie myalgie, syndrome d’hyperéosinophilie idiopathique, granulomatose éosinophilique avec polyangéite ou lymphome T cutané).
Données d'imageries
Utile lors du suivi, l’IRM est surtout l’examen de référence lors du diagnostic. Elle met en évidence une augmentation de l’intensité du signal du fascia sur les séquences T2 et rehaussement marqué après injection de gadolinium à la phase aiguë. L’échographie peut aussi être utile au diagnostic. Il existe une corrélation possible établie entre l’échographie des tissus mous et l’IRM musculaire dans la fasciite de Shulman. Une autre étude a montré une corrélation entre les résultats de l’échographie et l’amélioration clinique sous traitement corticoïde, suggérant l’utilisation de cette méthode pour le suivi des patients sous traitement.
Anatomopathologie
Le diagnostic de certitude reste l’examen anatomopathologique d’une biopsie cutanéo-fascio-musculaire. Cette biopsie doit être profonde, réalisée en un seul bloc, le plus précocement possible, idéalement avant la mise en route du traitement. Elle est toujours recommandée pour confirmer le diagnostic.
Elle révèle une fasciite : épaississement du fascia superficiel avec prolifération et hypertrophie des fibres de collagène, infiltrat inflammatoire composé de cellules mononuclées (lymphocytes, plasmocytes, histiocytes…) avec un regroupement périvasculaire. La présence de polynucléaires éosinophiles est fréquente mais inconstante et non indispensable au diagnostic.
Traitement
La corticothérapie reste la pierre angulaire du traitement. La dose initiale de traitement est habituellement de 0,7 mg/kg/jour. Les bolus intraveineux de corticoïdes permettraient d’obtenir un taux de rémission plus élevé et un recours moins fréquent à un traitement immunosuppresseur de deuxième intention.
En cas de corticodépendance, un traitement de fond peut être utile : méthotrexate le plus souvent (10 à 20 mg par semaine). D’autres traitements ont fait preuve de leur efficacité, notamment l’infliximab ou le rituximab.
(1) Interne des hôpitaux
(2) Service de rhumatologie, CHU Lariboisière (Paris)

CCAM technique : des trous dans la raquette des revalorisations
Dr Patrick Gasser (Avenir Spé) : « Mon but n’est pas de m’opposer à mes collègues médecins généralistes »
Congrès de la SNFMI 2024 : la médecine interne à la loupe
La nouvelle convention médicale publiée au Journal officiel, le G à 30 euros le 22 décembre 2024